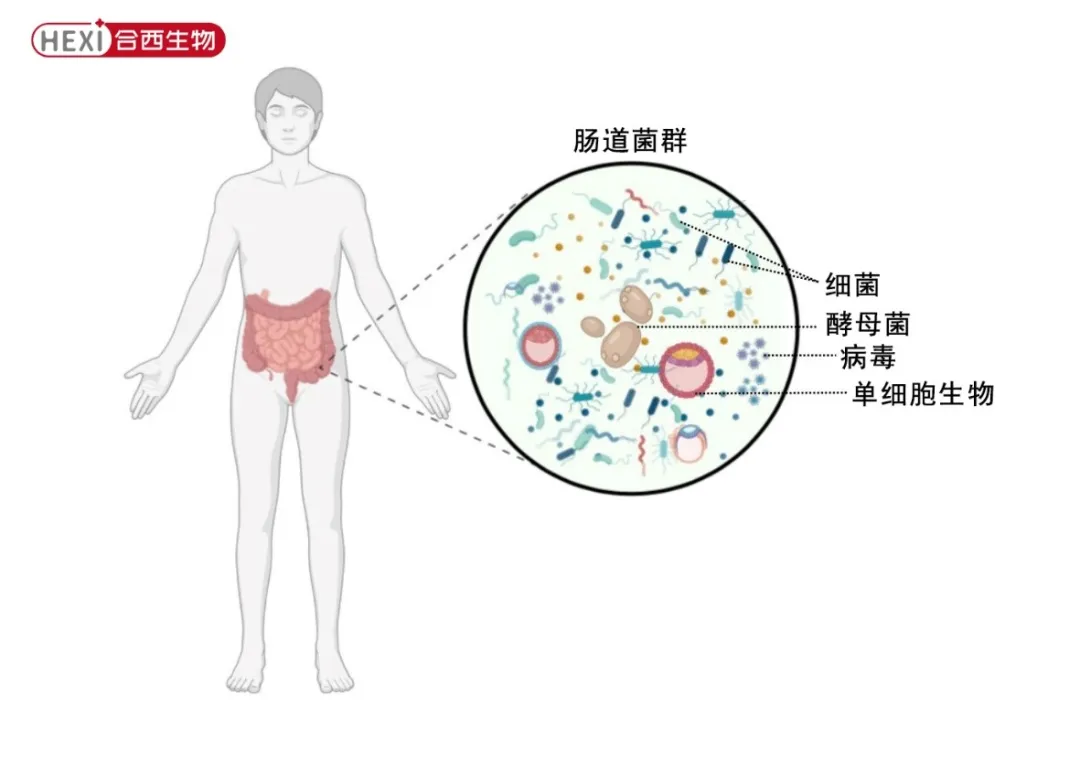
摘要:本综述讨论了富含脂肪和糖分、缺乏植物纤维的饮食习惯对肠道微生物菌群的不良影响。这导致肠道菌群失调和念珠菌属增殖,而念珠菌感染是世界范围内的主要真菌感染原因之一。除了不健康的饮食习惯,与疾病发展和肠道菌群失调有关的其他因素还包括吸烟、过量饮酒、缺乏体育锻炼、长时间使用抗生素和慢性心理压力。本综述建议,多样化的膳食,包括富含植物纤维、Omega-3多不饱和脂肪酸、维生素D和E以及与益生菌或后生元补充剂相关的微量营养素,可以改善肠道微生物群的生物多样性,促进短链脂肪酸的产生,并减少肠道内真菌物种的丰度。本综述还讨论了传统医学中对抗真菌过度生长和肠道菌群失调有效的各种食物和植物。总的来说,健康的饮食和生活方式因素有助于人类福祉,并增加肠道微生物群的生物多样性,从而对大脑和中枢神经系统产生积极调节作用。人类肠道微生物群包括100万亿种不同类型的微生物,包括细菌、病毒、真菌和单细胞生物。约99%的肠道细菌属于四个门类——厚壁菌门、拟杆菌门、变形菌门和放线菌门。一个健康个体的肠道微生物群以两个门类为主,即拟杆菌门和厚壁菌门。消化道的不同部位含有不同数量和类型的细菌。胃和上肠道中只有少量细菌存在,而从空肠到结肠,细菌数量逐渐增多。肠道微生物群被认为提供多种健康益处,包括病原体保护、营养代谢和免疫增强。人类健康取决于人体宿主与肠道微生物群之间的共生相互作用。然而,当肠道微生物群的组成和功能发生不良改变时,就会发生肠道菌群失调(图1)。本文综述了不同不健康饮食模式以及促进白色念珠菌在消化道中过度生长的因素,讨论了遵循健康饮食和生活方式如何增强免疫反应以对抗白色念珠菌,并减少与肠道菌群失调相关的炎症性疾病。该综述还关注食用低蔬菜纤维、高脂肪的不良影响,这会促进肠道菌群失调和真菌过度生长,尤其是白色念珠菌。除了不平衡的饮食,还有其他因素如吸烟、过度饮酒、缺乏运动、长期使用抗生素和慢性心理压力与疾病发展和肠道菌群失调相关。本综述还提出通过减少饱和/反式脂肪,增加多不饱和脂肪(特别强调欧米茄-3脂肪酸)来改善生活方式和不健康饮食的策略。这些策略强调了整个植物食物对肠道菌群失调和白色念珠菌过度生长的影响,包括膳食纤维、微量营养素、维生素、发酵蔬菜、益生菌和传统草药。这些健康饮食和生活方式因素已被证明有助于人类健康和福祉,并有助于改善肠道微生物组,进而对中枢神经系统和大脑产生积极影响(图1)
图1. 人类肠道菌群的示意图,其中包含1万亿个微生物,如细菌、病毒、真菌和单细胞生物,它们是肠道菌群的一部分。
白色念珠菌在肠道的寄生与炎症性疾病有关吗?
白色念珠菌是全球真菌感染的重要原因。这种酵母可以引发浅表性、全身性或侵袭性感染,后果严重。肠道菌群的改变、上皮屏障破裂和免疫系统功能障碍均促进了白色念珠菌从肠道过渡到重要器官。因此,消化道的状态是导致严重白色念珠菌感染的易感因素,这种感染在临床和社会经济意义上具有很高的重要性,是最常见的院内病原体之一。白色念珠菌通过其细胞壁与宿主相互作用,细胞壁是其主要接触点。真菌细胞壁保护酵母免受环境应激的影响,并维持其细胞完整性。这些应激包括温度和渗透压的剧烈变化、脱水以及免疫反应。真菌细胞壁成分对形态发生和致病性都至关重要,并且可能成为新的抗真菌药物的靶点。
白色念珠菌的细胞壁是由不同层次组成的动态结构。这个细胞壁包含深层的壳聚糖和密集层的中间β-1,3-和β-1,6-葡聚糖。壳聚糖是一种N-乙酰葡萄糖同聚物,具有1,4键连接,呈反平行折叠,并在其链上形成氢键。白色念珠菌细胞壁的内部骨架由壳聚糖微纤维链共价附着到β-1,3-葡聚糖上。磷酸肽甘露糖(PPM)覆盖在白色念珠菌细胞壁的表面,但与之没有共价连接。白色念珠菌细胞壁合成β-甘露糖,与PPM中的α-甘露糖相关联。这些甘露糖选择性地存在于一个名为磷脂甘露糖的分泌糖脂中,其与PPM细胞壁表面非共价关联。白色念珠菌细胞壁与宿主细胞的相互作用对真菌寄生于宿主以及激活促进感染的不同过程至关重要。
白色念珠菌在消化道中的过度生长被认为受到多种因素的影响,下文将讨论尤其是长期使用抗生素和不健康饮食模式。从单细胞酵母到纤维类菌丝形态的形态变化对白色念珠菌的毒力至关重要。在感染过程中,白色念珠菌酵母细胞通过依赖于吞噬细胞的机制传播到宿主的其他部位,中性粒细胞和巨噬细胞在这个过程中促进了传播,而菌丝则侵入和破坏宿主细胞。菌丝在巨噬细胞内的形成与吞噬体的破坏有关,通过抑制吞噬体酸化促进巨噬细胞的细胞死亡。在抗真菌免疫中,白色念珠菌特异性的Th17细胞能够防止真菌过度生长,并增强被皮肤组织寄生的上皮屏障完整性。此外,IL-22以及IL-17A和IL-17F由抗真菌的Th17细胞产生,它们增强了屏障功能,并保护肠道免受肠道损伤。对IL-17/IL-22信号通路在抗真菌免疫中的作用来说,其功能损害使个体易患粘膜-皮肤念珠菌病,但如果17型/1型免疫功能受损,也会发生相同的感染。关于IL-17在社会行为中的作用,真菌在肠道寄生促进小鼠的社会行为,无论是否存在细菌群落。这些发现表明真菌通过神经元中的IL-17R依赖性信号直接参与肠-脑轴。
另一个重要方面是白色念珠菌寄生与炎症性疾病的关系。实验和临床证据表明,白色念珠菌与克罗恩病(CD)之间可能存在联系,后者是一种慢性经肠壁的炎症性肠病(IBD)。CD通常影响回肠末端和结肠,但也可能影响消化道的其他部位。CD患者体内观察到抗真菌细胞壁多糖的高水平抗体(称为抗酿酒酵母抗体或ASCA),这些抗体能够识别白色念珠菌。此外,白色念珠菌在CD患者的粪便中更频繁地被分离出。在一个实验模型中评估了白色念珠菌过度生长对黏膜损伤的作用,这是由二氧化硫硫酸钠(DSS)引起的小鼠结肠炎模型。在这个DSS模型中,白色念珠菌加重了小鼠的结肠炎症,并且由DSS引起的结肠预炎增加了白色念珠菌的过度生长。白色念珠菌过度生长随后导致ASCA生成,这表明循环中的白色念珠菌甘露糖可以触发肠道炎症中的糖链抗体产生。与白色念珠菌类似,DSS引起的结肠炎小鼠中光滑念珠菌的丰度也显著升高。这种高丰度与炎症反应增加和微生物多样性减少相关。这表明真菌通过IL-17R依赖的信号在肠道炎症中直接参与肠-脑轴。这表明光滑念珠菌的丰度有助于维持肠道的菌群失调和炎症。
来自一些国家和烹饪传统的饮食,如地中海、冲绳和北欧饮食,都包含大量的整体植物食物(如蔬菜、水果和整粒食物),与较低的疾病风险相关。饮食和生活方式正在迅速传播,导致肥胖和文明病(糖尿病、心血管疾病、癌症等)的快速增加。此外,不健康的高脂肪和高糖,特别是加工食品,会引起与肠道炎症相关的肠道菌群变化。食品的加工过程包括去壳、加热和添加防腐剂,这些都会影响食物中存在的微生物。加热过程和添加防腐剂可以帮助减少致病菌和腐败菌,从而确保食物的安全性和延长保质期。然而,这些措施减少了有益的与食物相关的微生物的摄入。值得注意的是,加工食品和高脂肪饮食与菌群失调有关,包括拟杆菌门丰度的降低和厚壁菌门和变形菌门丰度的增加在小鼠模型中。这种高脂肪饮食会增加产生脂多糖(LPS)的细菌种群,如肠杆菌科,同时减少抑制LPS的细菌种群,如双歧杆菌。此外,这种饮食会影响上皮细胞,导致肠道屏障的改变,包括肠道通透性增高和从肠道进入血液的LPS转位。脂肪摄入的增加,特别是长链脂肪酸,可以触发肠淋巴细胞、上皮细胞内淋巴细胞、树突状细胞和肠上皮细胞的炎症细胞因子的释放。低脂肪但富含纤维的饮食可以减少溃疡性结肠炎患者的炎症和菌群失调,并改善他们的生活质量。在他们的临床研究中,分析了自养、超重和肥胖个体的不同样本中可培养真菌的部分。肥胖者身体中的真菌物种数量比自养者更高。此外,白色念珠菌是肥胖者中最常见的酵母菌。就富含糖的饮食而言,摄入简单的糖会降低肠道微生物群的生物多样性,并减少肠腔中的短链脂肪酸(SCFAs)。一项实验研究显示,饮用高糖饮食的小鼠肠道通透性、脾脏重量和中性粒细胞水平显著增加。在接受DSS治疗后,这些小鼠迅速发展出严重的结肠炎。此外,这些小鼠的粪便样本显示出肠道病原菌(如大肠杆菌和白色念珠菌)显著增加。整体植物食物含有可发酵膳食纤维,它是食物中无法被小肠内源酶消化的部分。在大肠中,肠道菌群可以将可发酵纤维转化为各种小有机代谢物,其中最为重要的是短链脂肪酸(SCFAs)。乙酸、丙酸和丁酸是SCFAs,具有抗炎、抗氧化和抗癌的特性。例如,在这些整体植物食物中,整粒谷物含有复杂的膳食纤维组成,如阿拉比诺木聚糖和β-葡聚糖,这些成分有助于增加SCFA的产生。在低动物脂肪和蛋白质但高纤维的饮食中,SCFAs为结肠细胞提供额外的能量。SCFAs与G蛋白偶联受体(GPCRs),如GPR41(游离脂肪酸受体3;FFAR3)和GPR43(FFAR2)结合,这些受体表达在肠内内分泌L细胞上。这进一步触发胰高血糖素样肽1和多肽YY的分泌,从而增加能量消耗、减少食物摄入,并改善葡萄糖代谢和胰岛素分泌。消费较多的零食和垃圾食品的特点是支链脂肪酸(BCFAs)在粪便中的水平较高,这反映了动物蛋白质的细菌分解代谢。在这种富含脂肪和蛋白质的饮食中,细菌酶首先解离复杂蛋白质,释放出游离氨基酸和短肽,然后经过发酵。蛋白质发酵的增加、BCFAs(如异丁酸和异戊酸)、有机酸和气体引起菌群失调,并导致病原体来源化合物的泄漏,包括血液中LPS水平的增加,从而引发炎症和胰岛素抵抗。关于SCFAs的抗真菌活性,肠道菌群产生的代谢产物对白色念珠菌具有抗真菌活性。丁酸钠可以减少白色念珠菌的生长和菌丝形成。此外,当暴露在白色念珠菌感应下时,巨噬细胞的抗菌活性会增强。Garcia等人证明,肠道菌群代谢产物可以抑制白色念珠菌的菌丝形成和真菌对人结肠上皮的侵袭。导致炎症发病和肠道菌群失调的因素
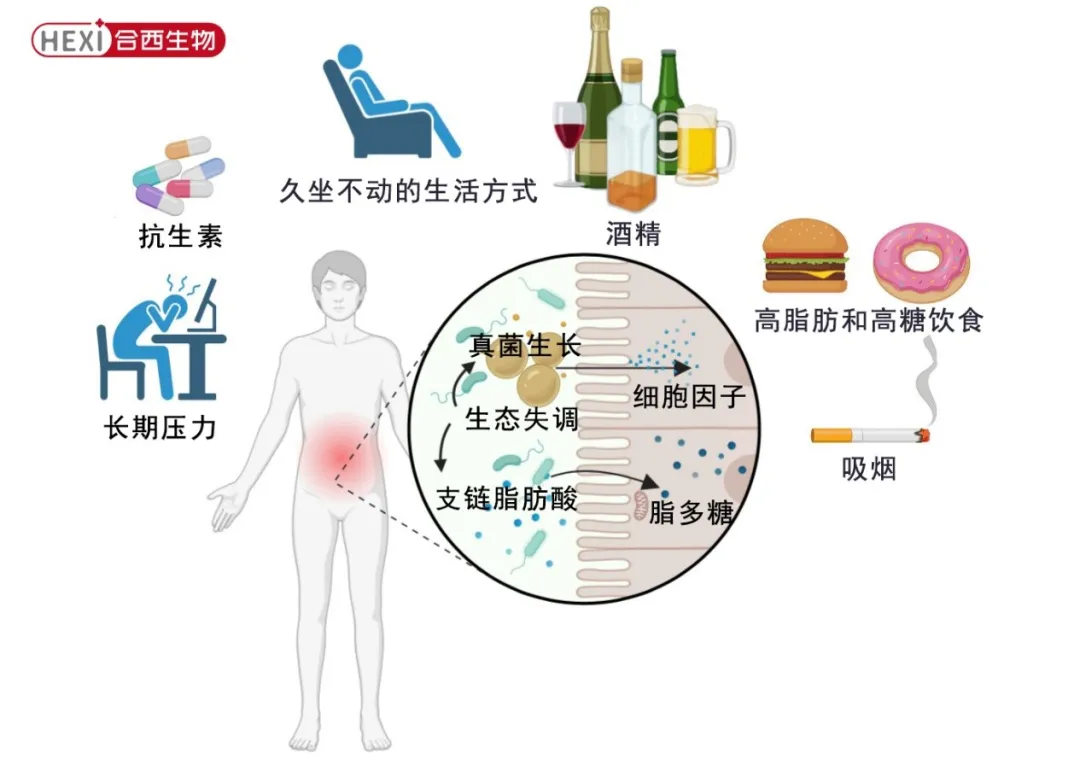
如上所述,不健康的饮食模式并不是导致炎症发病的唯一生活方式因素;吸烟、过度饮酒、缺乏体育锻炼、长期使用抗生素和慢性心理压力都会导致疾病的发展和肠道菌群失调(图2)。

图2. 不健康饮食模式导致炎症发病和肠道菌群失调的示意图。高脂肪和高糖饮食、吸烟、过度饮酒、缺乏体育锻炼、长期使用抗生素和慢性心理压力都会导致肠道菌群失调的发展。这些饮食模式会导致支链脂肪酸(BCFA)的产生增加和光合菌群细菌(如大肠杆菌)的增多,它们产生脂多糖(LPS),同时会改变肠道屏障。在菌群失调的情况下,还观察到真菌明显过度生长,特别是白色念珠菌。所有这些因素会导致促炎细胞因子的产生和病原来源化合物(包括LPS和真菌细胞壁成分)的泄漏到血液中。
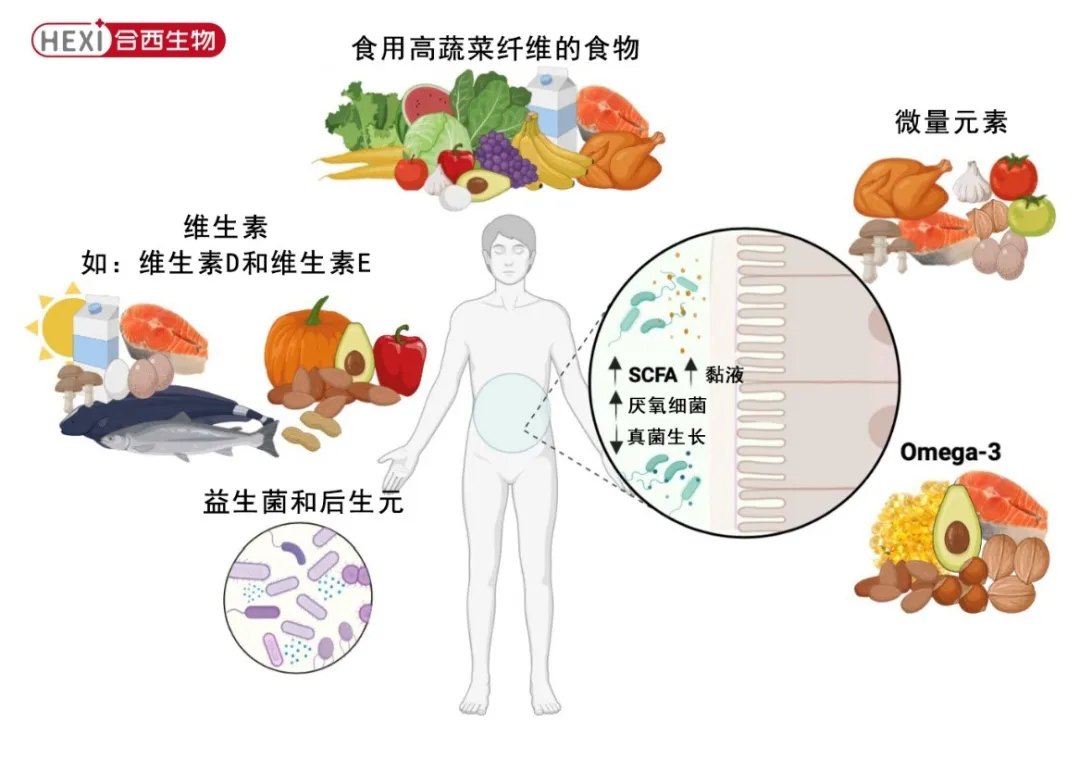
压力是一系列威胁身体内稳态的事件,由外部或内部因素(压力因素)引起。研究表明,暴露于社会压力因素会改变结肠菌群的稳定性,导致细菌移位和免疫反应,相对富集的拟杆菌属的相对丰度减少,梭状芽孢杆菌的相对丰度增加。一项实验研究显示,感染白色念珠菌并暴露于慢性不同种类的应激的大鼠,肝脏和肾脏中的真菌负担增加。此外,巨噬细胞产生的一氧化氮显著减少,说明慢性不同种类应激影响了巨噬细胞对白色念珠菌的吞噬能力。过度饮酒是许多健康问题的主要风险因素。小鼠的慢性酒精摄入增加了真菌群落的数量,并促进真菌β-葡聚糖进入血液循环,而抗真菌药物的治疗减少了肠道真菌的负荷,降低了β-葡聚糖的迁移,并改善了酒精引起的肝脏损伤。在随后的临床研究中,与酒精相关的肝病患者的真菌多样性较低,并显示出念珠菌物种的富集。此外,血清ASCA水平与酒精性肝炎患者的死亡率增加相关,表明治疗肠道真菌可能对酒精性肝炎患者有益,ASCA可能有助于预测其预后。长期使用抗生素来对抗传染性疾病也是微生物丰富度和多样性改变的一个因素(图2)。一些共生和共生菌在短期内接受广谱抗生素治疗后会减少。抗生素会清除保护性微生物群落,使环境更有利于念珠菌的生长。研究发现长期使用抗生素增加了外阴阴道念珠菌病的风险,而这种风险与抗生素的使用持续时间而不是类型直接相关。在实验小鼠模型中,抗生素治疗长期减少了小鼠中的拟杆菌科菌群,但在抗生素恢复期间存在白色念珠菌促进了拟杆菌科菌群的恢复。然而,白色念珠菌随时间的推移减少了乳酸菌的物种,并促进了肠球菌的生长,这表明白色念珠菌的丰富维持了肠道细菌群的紊乱。临床研究显示,在接受抗生素治疗的健康志愿者的粪便样本中白色念珠菌的水平增加。吸烟会减少唾液产量,改变口腔微生物群落,并增加口腔念珠菌的定植。研究表明,吸烟者患口腔念珠菌感染的风险增加了7倍。吸烟者患有活动龋病损的口腔中更容易存在念珠菌。人们认为,由于中性粒细胞对真菌的活性减少,吸烟者更容易出现白色念珠菌定植的高发生率。此外,吸烟会减少牙龈沟液的量,其中含有抗体和白细胞。缺乏IL-1β的小鼠在接触烟雾时高度定植白色念珠菌,并且生存率比野生型小鼠更低。缺乏体育锻炼会对多种健康结果产生影响,并引发系统性炎症的不同循环标志物的活化(C-反应蛋白、IL-6、TNFα和新生物酶)。然而,定期进行体育锻炼可以改善生活质量,降低系统性炎症,并增强对感染的免疫反应。适度的运动可以增加年轻男性中中性粒细胞对白色念珠菌的吞噬能力。与该研究一致,自发运动、趋化性、自发附着和巨噬细胞对白色念珠菌的摄取在体育训练中显著增加,支持体育锻炼对巨噬细胞吞噬功能的有益影响。缺乏维生素D和E、硒等微量元素以及ω-3多不饱和脂肪酸与感染期间的负面临床结果相关。多样化的饮食富含植物纤维、维生素和微量营养素,结合益生菌/后生元补充剂,可以改善肠道微生物群和SCFA产生,并减少真菌负荷(图3)。
图3.高植物纤维、维生素、微量营养素、ω-3多不饱和脂肪酸和益生菌/后生元质饮食对肠道微生物群的有益影响的示意图。以蔬菜、水果、全谷物、坚果和种子为基础的全植物食物饮食,再结合一部分动物产品(肉类、乳制品和蛋类)或海鲜,可提供大量的纤维、抗氧化剂,以及维生素D、E、ω-3脂肪酸和硒等微量营养素。此外,益生菌或后生元补充剂对于防止肠道菌群失调至关重要。这种饮食有助于增加短链脂肪酸(SCFA)的产生和黏液分泌,以及乳酸菌和双歧杆菌等厌氧菌的增加。食用这种饮食的人群真菌病原显著减少。所有这些条件都有助于促进肠道微生物群的多样性。维生素D在皮肤暴露在阳光下后合成,或者通过某些鱼类、蛋黄、乳制品和蘑菇等食物获得。在一项临床试验中,维生素D3每天补充剂减少了曲霉菌引起的IL-13反应。维生素D3通过抑制白色念珠菌挑战的外周血单核细胞中TLR2、TLR4、Dectin-1和甘露糖受体的表达,调节细胞因子反应,使其朝向抗炎型,研究表明维生素D3具有杀真菌作用,这种维生素的脂溶性特性改变了真菌细胞膜的完整性,具有抗真菌特性。与这项研究一致,维生素D3影响了白色念珠菌的碳水化合物代谢和核糖体生物合成。在小鼠腹腔念珠菌病模型中,维生素D3减少了不同器官中的真菌负荷,降低了炎症细胞的浸润和IFN-γ和TNF-α的水平。维生素E是一种脂溶性化合物,存在于许多坚果、种子、蔬菜和油中。已经显示维生素E通过抑制NF-κB活性对白色念珠菌具有广泛的抗炎作用。在与两性霉素B相比,将维生素C和E添加到两性霉素B中可显著增加治疗效果。此外,当添加维生素C和E时,人类红细胞对两性霉素B引起的细胞毒性的保护作用,显示出这些维生素通过其抗氧化特性对两性霉素B引起的自氧化提供了保护作用。ω-3多不饱和脂肪酸含有亚麻酸(18:3 ω-3)、硬脂酸(18:4 ω-3)、二十碳五烯酸(EPA; 20:5 ω-3)、二十二碳五烯酸(22:5 ω-3)和二十二碳六烯酸(DHA; 22:6 ω-3)。海洋哺乳动物的脂肪和白鱼的肝脏含有EPA和DHA等长链脂肪酸。不同的研究表明EPA和DHA不仅对心脏、大脑和眼睛健康有益,还对免疫系统有益。有证据表明多不饱和脂肪酸及其酯衍生物对多种口腔病原菌具有抗菌作用,包括白色念珠菌。硒等微量营养素是一种微量元素,通过人类和动物消费的植物进入食物链。超过25种硒蛋白质包含硒,它具有抗氧化、化学预防、抗炎和抗菌作用。已经显示硒纳米颗粒能够附着在白色念珠菌生物膜上,然后渗透进入这种病原体。因此,硒纳米颗粒通过将硫替代硒来破坏白色念珠菌的细胞结构。在接受硒补充的小鼠中,与缺乏硒的小鼠相比,感染白色念珠菌的肝脏和脾脏中的真菌负荷明显增加。此外,硒缺乏还损害了小鼠中性粒细胞在体外实验中杀死白色念珠菌的能力。益生菌,包括细菌和酵母菌,被定义为在人体中展示出有益健康效果的活性微生物(图3)。目前的益生菌在我国已有安全名录,这些菌种都已被证明是安全的。益生菌已被证明能减少消化系统疾病的症状,如肠易激综合征、炎症性肠病以及具有难治性难题的艰难梭菌感染,还能改善情绪障碍,如抑郁症。益生菌与致病菌竞争营养和附着位点,改善菌群失调。此外,它们改善上皮细胞形成的屏障功能,调节免疫反应,并通过神经递质产生和免疫调节间接影响其他器官。已经显示乳酸菌能够在生物膜形成的定植和成熟阶段减少白色念珠菌生物膜。此外,乳酸菌可能通过竞争营养物质和产生乳酸和其他有机酸来抑制白色念珠菌的生长,从而降低pH值。因此,念珠菌的与压力相关的基因在不适宜的低pH环境中被上调。此外,益生菌发现能降低与麦角甾酮合成和氟康唑耐药外排泵相关的基因的表达。在菌群失调中,益生菌可以帮助恢复肠道中的健康菌。益生菌对微生物群营养活动中的交叉反馈很重要,影响其他共生菌的代谢能力。双歧杆菌可以代谢宿主饮食或粘膜中的不同类型的碳水化合物,其发酵途径产生不同水平的乙酸和乳酸酸。研究表明,高脂饮食会引起小鼠肠道菌群的显著变化,伴随肠道通透性、LPS渗透、炎症、葡萄糖耐受性受损和过食的改变。然而,用乳酸菌治疗完全逆转了与肥胖相关的这些特征,改变了肠道菌群的组成。与这项研究一致,用乳酸菌和双歧杆菌菌株治疗的肥胖小鼠体重和胆固醇水平较低。它们还患有较少的真菌感染,恢复了肝脏形态,并有益地调节了肠道菌群。通过摄入选择性益生菌,还可以调节大脑活动。接受干酪乳酸菌代田株菌株治疗2个月的慢性疲劳综合征患者显示乳杆菌和双歧杆菌的丰度显著增加,焦虑症状显著减轻。健康志愿者在摄入瑞士乳杆菌R0052和长双歧杆菌R0175两周后,焦虑和抑郁症状也得到缓解。后生元(即无生命菌体和/或其代谢产物的制剂),其中的寡糖,是被肠道细菌选择性代谢而不是被宿主代谢的可消化性碳水化合物(图3)。后生元补充剂是一种通过改变肠道微生物群的组成和/或活性来为宿主提供益处的膳食策略。此外,已经证明后生元能减轻与炎症性肠病、感染和抗生素引起的腹泻等症状有关的症状。在小鼠DSS诱导的结肠炎模型中,果寡糖补充剂减少了病理免疫反应,并防止了肠道屏障的结构损伤。研究表明果寡糖对预防阴道感染有效。不同的临床和实验研究探讨了β-葡聚糖(存在于燕麦、大麦、真菌和一些藻类中)和几丁质(存在于甲壳类动物和甲虫壳以及真菌细胞壁中)在预防肠道菌群失调中的后生元作用。通过在体内模型中给动物喂养β-葡聚糖和几丁质,可以增强双歧杆菌菌株的定植效率。将β-葡聚糖或几丁质口服给小鼠导致耐氧菌群,尤其是大肠杆菌和嗜肠球菌,以及真菌群的减少,而约氏乳杆菌和多形拟杆菌的群体在DSS诱导的结肠炎模型中显著增加。从这些研究可以明确看出,β-葡聚糖或几丁质在调节免疫反应和改善肠道微生物群多样性方面起着重要作用。繁忙的日常生活使许多人习惯了高脂肪高糖的饮食方式,以及在缺乏阳光的环境中形成久坐的习惯。此外,我们的日常生活常常导致我们经历慢性心理压力,进而导致不健康的习惯,如吸烟和饮酒,以及缺乏社交。以上因素严重影响了我们的肠道菌群,促进了肠道菌群失调,包括机会性念珠菌滥生和厌氧菌群(如双歧杆菌)种群的减少。然而,现在有越来越多的证据表明,健康的饮食选择和富含纤维的健康饮食可以预防许多与慢性炎症相关的疾病,如炎症性肠病。本综述讨论了导致肠道菌群失调和肠道病原菌过度生长的因素,并提出了健康饮食模式可能改善肠道菌群的多样性的建议,同时概述了各种食物和植物,在传统医学中以抗击真菌过度生长和肠道菌群失调而闻名。综合考虑所有这些因素,证据表明,多样化的膳食,包括富含植物纤维、Omega-3多不饱和脂肪酸、维生素D和E以及与益生菌或后生元补充剂相关的微量营养素,有助于改善人类福祉,同时增加肠道菌群的多样性,从而对中枢神经系统(CNS)和大脑产生积极影响。(相关参考:合西生物丨益生菌治疗神经退行性疾病的系统综述)本文献原文自 MDPI· 《Healthy Diet and Lifestyle Improve the Gut Microbiota and Help Combat Fungal Infection》.